Сроки выдачи разрешений на клинические исследования рекордно увеличились

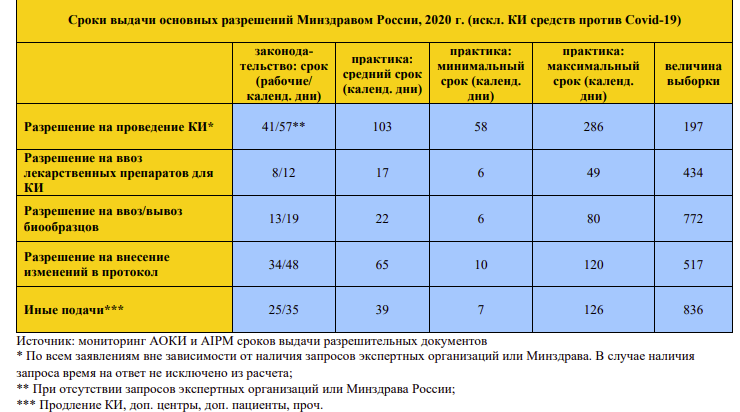
Средняя длительность рассмотрения заявлений на клинические исследования в России существенно выросла: с 87 до 103 дней. Аналогичная тенденция отмечалась при внесении изменений в протокол испытания, выдаче разрешений на ввоз препаратов, ввоз и вывоз биологических образцов. Это следует из отчета за 2020 год Ассоциации организаций по клиническим исследованиям (АОКИ), с которым ознакомился «ФВ».
Средний срок внесения изменения в протокол составил 65 дней по сравнению с 48 днями в 2019 году. В меньшей степени изменение сроков коснулось выдачи разрешений на ввоз и вывоз препаратов и образцов: они увеличились в среднем с 15 до 17 дней для лекарств, с 20 до 22 — для биологических образцов, говорится в отчете.
Последний раз столь длительные сроки выдачи разрешений наблюдались в 2011—2012 годах. Тогда проходила реформа регуляторной системы после вступления в силу нового Федерального закона № 61 «Об обращении лекарственных средств».
Однако увеличение сроков не коснулось исследований при COVID-19. Средняя длительность рассмотрения заявлений на исследование противокоронавирусных препаратов составила 25 дней. При этом минимальный срок получения решения Минздрава на исследование при COVID – 10 дней, указано в отчете АОКИ.
Также в отчете говорится, что пандемия COVID-19 негативно сказалась на локальных клинических исследованиях иностранных спонсоров: их число сократилось почти вдвое. Однако общее число международных многоцентровых испытаний не изменилось по сравнению с 2019 годом.


























Нет комментариев
Комментариев: 0